Ths.Bs Lê Minh Tuấn, PGS.TS.BS Lê Trọng Bỉnh, Khoa Chẩn đoán hình
PGS.TS.BS Đặng Công Thuận, Khoa Giải phẫu bệnh
Bệnh viện Trường Đại học Y-Dược Huế
GIỚI THIỆU
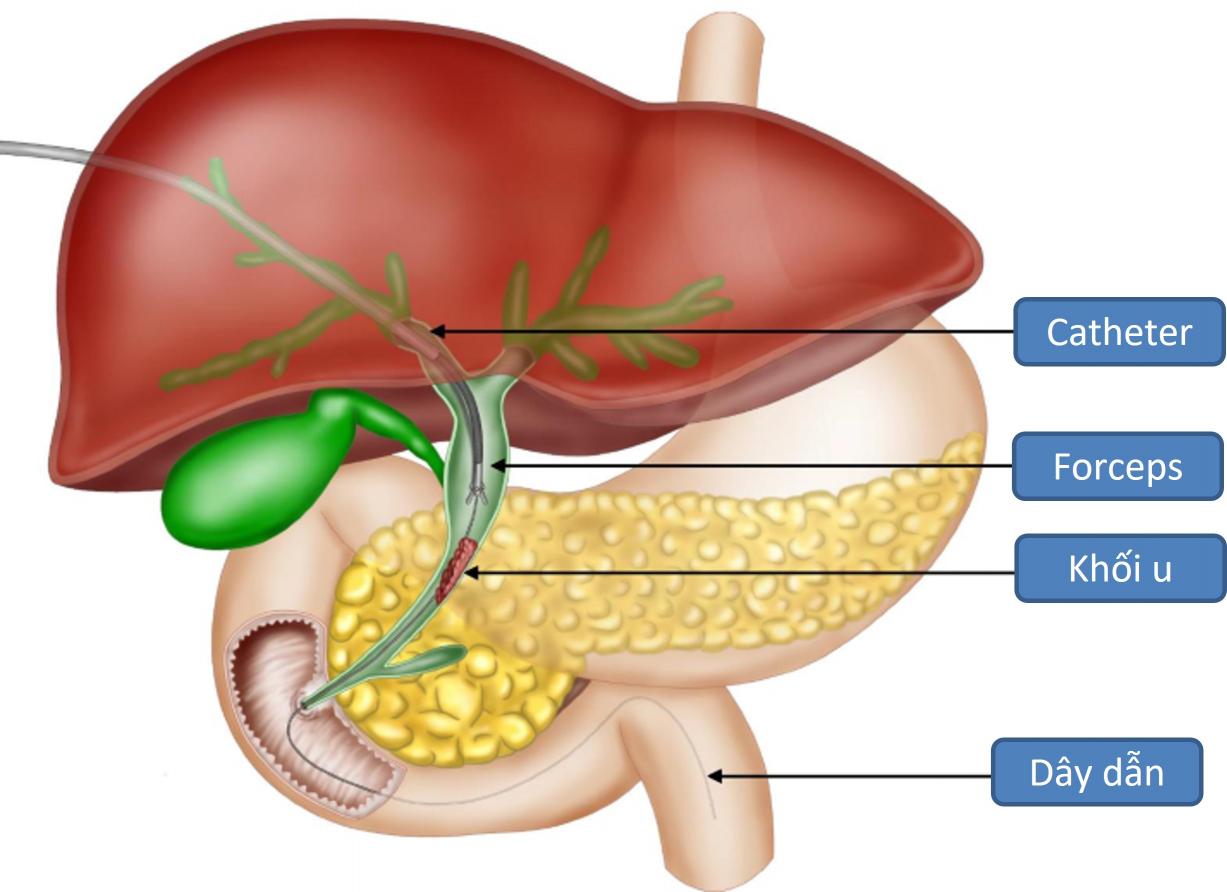
Vừa qua, Bệnh viện trường Đại học Y-Dược Huế đã triển khai thành công kỹ thuật sinh thiết lõi tổn thương trong lòng đường mật qua da bằng forceps (Hình 1). Đây là một kỹ thuật mới, cung cấp thêm một giải pháp để lấy mẫu bệnh phẩm chẩn đoán trong những trường hợp vàng da tắc mật phức tạp, có tổn thương nằm sâu trong ổ bụng, tổn thương ở vị trí khó tiếp cận qua nội soi hay qua da. Việc triển khai thành công kỹ thuật này sẽ mở ra cơ hội điều trị trúng đích cho nhiều bệnh nhân tắc mật ác tính.
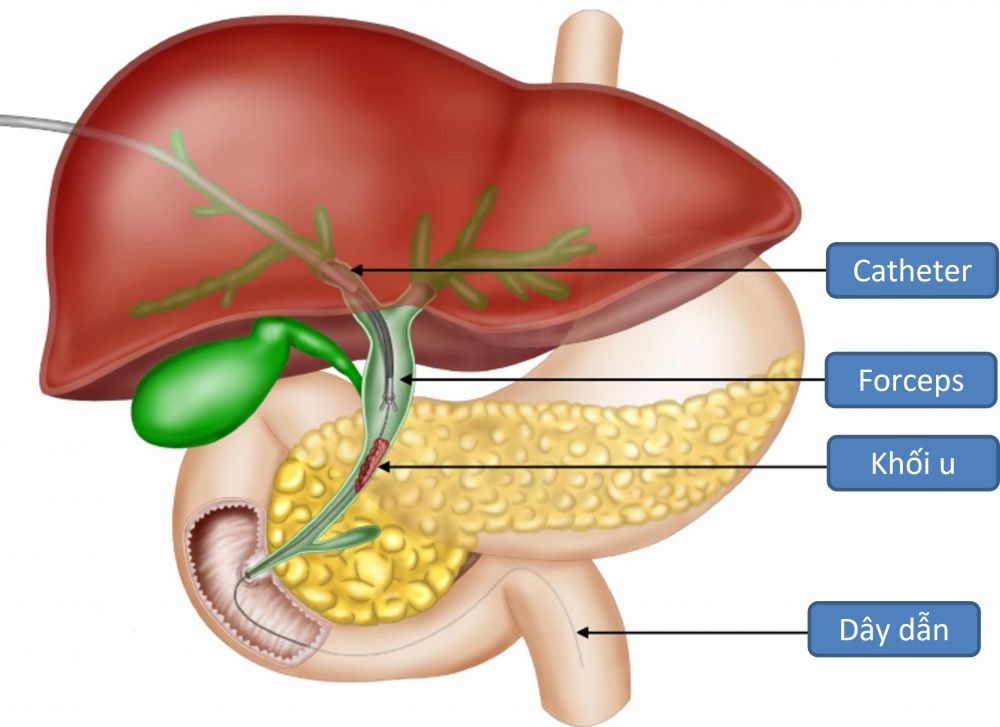
Hình 1. Minh hoạ kỹ thuật sinh thiết lõi khối u trong lòng đường mật bằng forceps
TRƯỜNG HỢP MINH HOẠ
Trường hợp 1
Bệnh nhân nam, 70 tuổi, nhập viện khoa Ngoại Tiêu hoá vì vàng da, vàng mắt, mệt mỏi nhiều. Kết quả xét nghiệm cho thấy tình trạng tắc mật rõ: Bilirubin toàn phần 153 µmol/l, bilirubin trực tiếp 112,7 µmol/l. Hình ảnh siêu âm và CLVT cho thấy khối u ở đầu tuỵ, xâm lấn đoạn cuối ống mật chủ gây tắc hoàn toàn đường mật trong gan và ngoài gan, đồng thời có nhiều nốt nhỏ rải rác khắp nhu mô gan, nghi ngờ tổn thương di căn gan đa ổ (Hình 2).
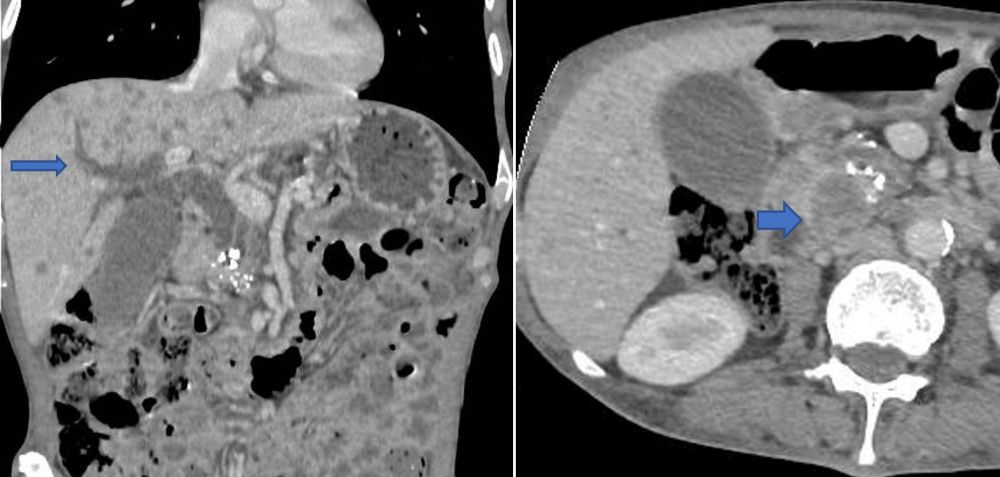
Hình 2. Khối u vùng đầu tuỵ (mũi tên) ngắn chèn ép gây giãn đường mật trong gan (mũi tên dài).
Sau khi hội chẩn đa chuyên khoa, bệnh nhân được chỉ định dẫn lưu đường mật xuyên gan qua da (PTBD: percutaneous transhepatic biliary drainage) nhằm giảm áp đường mật, cải thiện toàn trạng và sẽ được tiến hành đặt stent tái thông đường mật thì hai. Vì đã quá giai đoạn phẫu thuật triệt căn nên việc xác định chính xác bản chất của khối u có ý nghĩa quyết định đến hướng điều trị sau này của bệnh nhân sau khi đã đặt stent tái thông đường mật. Nhận định tổn thương này nằm ở vùng đầu tuỵ, sâu trong ổ bụng, phía trước có nhiều cấu trúc ống tiêu hoá che lấp, xung quanh có nhiều mạch máu lớn, toàn trạng bệnh nhân nặng nên không phù hợp để tiến hành sinh thiết qua da dưới hướng dẫn siêu âm hay CLVT. Do đó, chúng tôi chọn phương pháp sinh thiết khối u trong lòng đường mật qua da bằng forceps qua da, tận dụng đường hầm đã có sẵn tron quá trình dẫn lưu đường mật qua da.
Thủ thuật:
Chọc đường mật ngoại vi xuyên gan dưới hướng dẫn của siêu âm, luồn dây dẫn và đặt ống thông vào đường mật. Đặt dẫn lưu đường mật vào ống mật chủ. Sau 1 tuần dẫn lưu, toàn trạng của bệnh nhân tiến triển tốt, vàng da giảm rõ, xét nghiệm bilirubin máu giảm rõ (Bilirubin toàn phần: 46,3 µmol/l, Bilirubin trực tiếp 34,4 µmol/l).
Chụp đường mật cản quang, đưa catheter 8F tiếp cận vị trí tổn thương dưới hướng dẫn của máy chụp mạch xoá nền. Đưa forceps vào tổn thương qua catheter, lấy mẫu khối u ở nhiều vị trí. Sau sinh thiết, tiến hành đặt stent tái thông đường mật theo như kế hoạch đã đề ra (Hình 3). Trong và sau các thủ thuật không xảy ra tai biến.
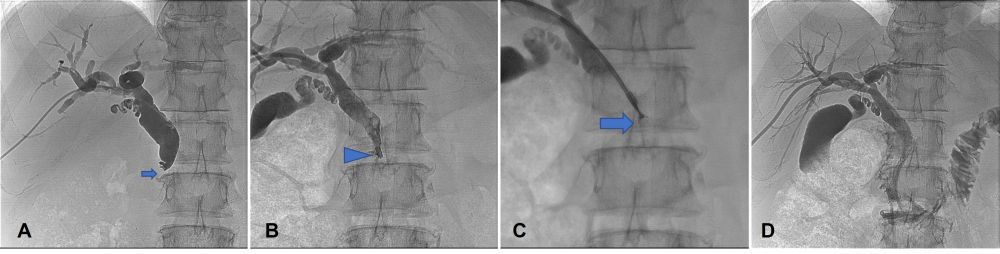
Hình 3. Sinh thiết và đặt stent đường mật. (A) Chụp đường mật qua da: cắt cụt hoàn toàn ống mật chủ (mũi tên ngắn), không thấy thuốc cản quang thông xuống tá tràng. (B) Đưa catheter tiếp cận vị trí khối u. (C) Lấy mẫu khối u bằng forceps. (D) Đặt stent tái thông hoàn toàn đường mật.
Các mẫu sinh thiết đều đạt tiêu chuẩn chẩn đoán mô bệnh học. Kết quả hoá mô miễn dịch phù hợp carcinoma thần kinh nội tiết xâm nhập (Hình 4). Bệnh nhân được hội chẩn liên chuyên khoa để tiến hành các bước điều trị tiếp theo tại Khoa Ung bướu.
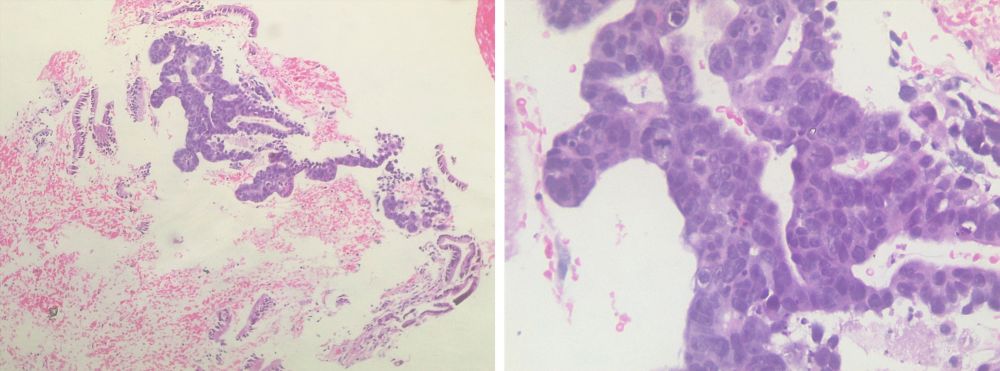
Hình 4. Hình ảnh vi thể phù hợp carcinoma thần kinh nội tiết xâm nhập.
Trường hợp 2
Bệnh nhân nam, 58 tuổi, nhập viện khoa Ngoại Tiêu hoá vì vàng da, vàng mắt, chán ăn. Kết quả xét nghiệm ghi nhận tình trạng tắc mật nặng: Bilirubin toàn phần 299,8 µmol/l, bilirubin trực tiếp 210,5 µmol/l. Hình ảnh cộng hưởng từ gan mật cho thấy khối u dạng thâm nhiễm ở rốn gan, xâm lấn, cắt cụt đường mật đoạn hợp lưu ống gan trái-phải, lan vào đường mật trong gan và hợp lưu phân thuỳ trước-sau gây giãn lớn đường mật thượng lưu kèm viêm đường mật (Hình 5).
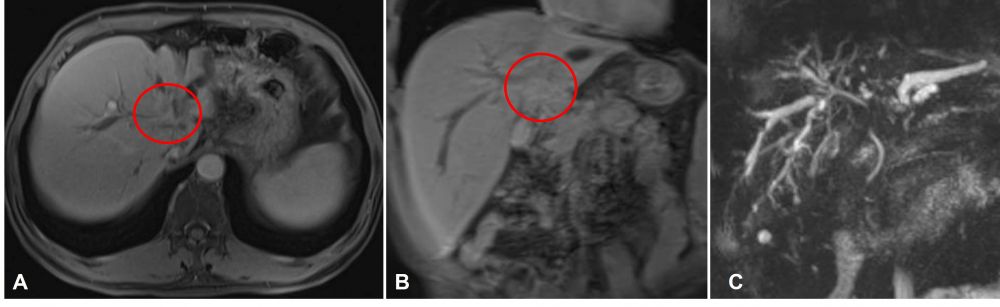
Hình 5. Hình ảnh cộng hưởng từ khối u ở vùng rốn gan (vòng đỏ) xâm lấn đường mật trong gan và hình ảnh tái tạo MRCP, tương ứng với u Klatskin type IV
Tương tự trường hợp trên, bệnh nhân được chỉ định dẫn lưu đường mật qua da để giảm áp và cải thiện triệu chứng. Trong quá trình dẫn lưu, chúng tôi kết hợp sinh thiết khối u trong lòng đường mật để lấy mẫu bệnh phẩm (Hình 6). Trong và sau thủ thuật không xảy ra tai biến. Bệnh nhân tiếp tục được theo dõi tại bệnh phòng, tình trạng tắc mật cải thiện dần, bilirubin TP: 194,7 µmol/l; bilirubin TT: 140,7 µmol/l và được đặt stent đường mật qua da sau 1 tuần (Hình 7).
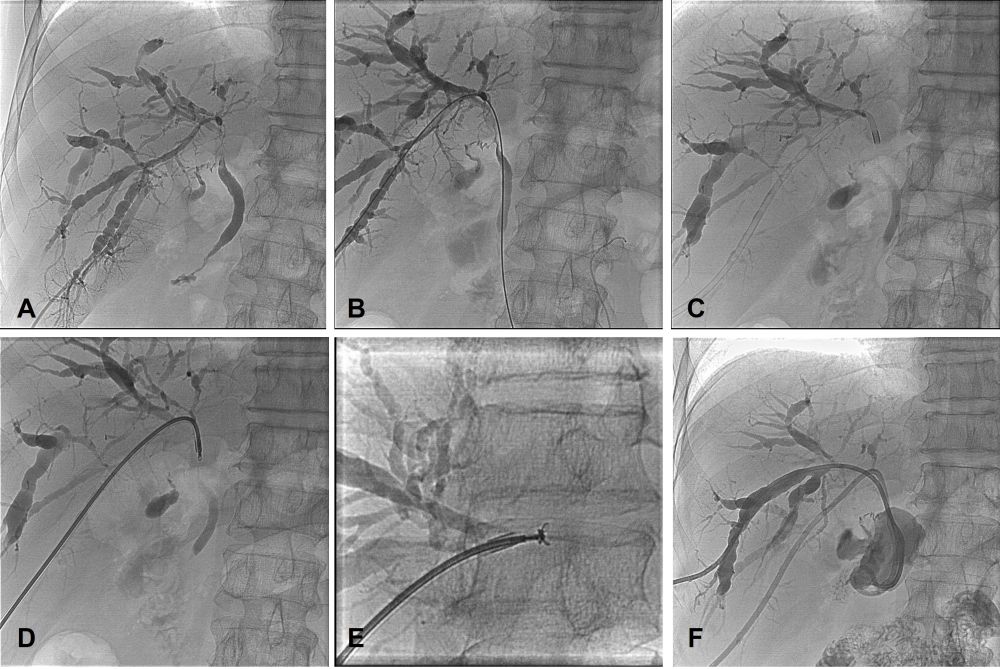
Hình 6. Dẫn lưu đường mật qua da và sinh thiết trong lòng đường mật. (A) Chụp đường mật: hẹp nham nhở đường mật trong gan từ đoạn hợp lưu phân thuỳ đến ống mật chủ, tắc hoàn toàn ống gan trái. (B) Luồn dây dẫn qua chỗ tắc. (C) Đưa catheter tiếp cận tổn thương. (D) Đưa forceps vào vị trí lấy mẫu. (E) Lấy mẫu bằng forceps. (F) Đặt 2 dẫn lưu qua da cho phân thuỳ trước và phân thuỳ sau.
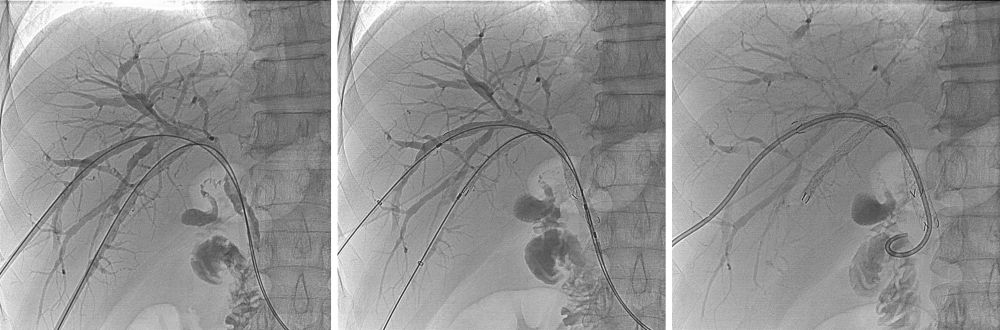
Hình 7. Đặt kissing stent đường mật qua da từ 2 nhánh phân thuỳ trước và phân thuỳ sau để tái thông hoàn toàn đường mật gan phải.
Mẫu sinh thiết lõi đạt tiêu chuẩn chẩn đoán với kết quả mô bệnh học phù hợp ung thư biểu mô tuyến đường mật xâm nhập (Hình 8). Bệnh nhân được chuyển sang Khoa Ung bướu để tiếp tục điều trị.
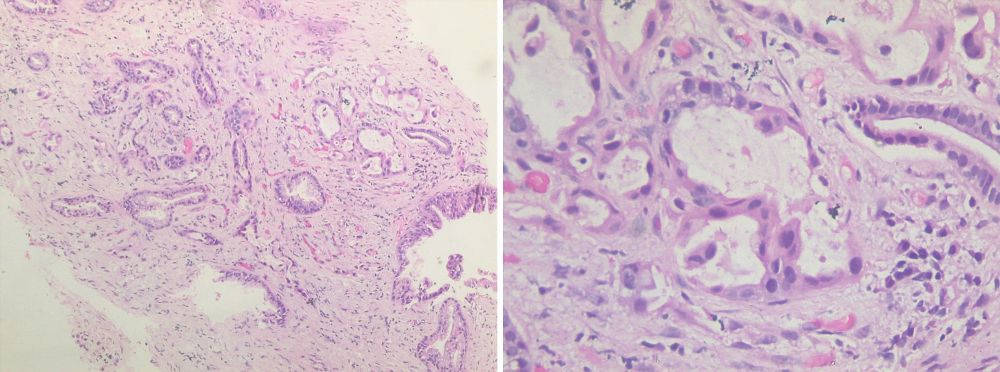
Hình 8. Hình ảnh mô bệnh học phù hợp ung thư biểu mô tuyến đường mật xâm nhập
BÀN LUẬN
Vàng da tắc mật do các khối u ác tính xâm lấn, chèn ép đường mật là một nhóm bệnh lý ác tính khá phổ biến, gây ra bởi nhiều nguyên nhân như ung thư tuỵ, ung thư đường mật đoạn xa, ung thư gan, ung thư bóng Vater, ung thư dạ dày-tá tràng, hoặc hạch di căn....(2) Bệnh nhân thường được phát hiện muộn do triệu chứng sớm mơ hồ, không đặc hiệu, bệnh tiến triển nhanh, điều trị khó khăn và có tiên lượng không tốt. Bệnh nhân thường vào viện với các triệu chứng vàng da, vàng mắt, mệt mỏi, đau âm ỉ vùng thượng vị, chán ăn, thậm chí suy kiệt (3). Nhiều nghiên cứu cho thấy chỉ khoảng 20% bệnh nhân có thể chỉ định phẫu thuật triệt căn ở thời điểm được chẩn đoán (4), (5).
Chẩn đoán vàng da tắc mật, vị trí tắc, mức độ tắc và định hướng nguyên nhân gây tắc mật đã và đang được thực hiện thường quy với các phương tiện chẩn đoán hình ảnh không xâm nhập như siêu âm, cắt lớp vi tính (CLVT) và cộng hưởng từ (CHT). Tuy nhiên, các tổn thương ác tính trong lòng đường mật (intraductal), tổn thương quanh ống mật (periductal) thường có kích thước nhỏ, lan dọc theo ống mật nên khó phát hiện bằng hình ảnh và khó phân biệt với các tổn thương lành tính khác (6). Ngoài ra, các khối u ở vùng quanh bóng Vater như ung thư đường mật, ung thư tuỵ, ung thư bóng Vater, ung thư tá tràng thường có biểu hiện lâm sàng và đặc điểm hình ảnh học tương tự nhau. Do đó, việc chẩn đoán xác định bản chất của tổn thương đòi hỏi phải lấy được mẫu mô của tổ chức u (sinh thiết lõi) để làm các xét nghiệm mô bệnh học, hoá mô miễn dịch và sinh học phân tử. Kết quả giải phẫu bệnh này chính là nền tảng cho các phương pháp điều trị sau này cho bệnh nhân.
Bệnh viện trường Đại học Y Dược Huế đã triển khai nhiều kỹ thuật sinh thiết lõi khối u phổ biến hiện nay là sinh thiết qua nội soi tiêu hoá, siêu âm nội soi, sinh thiết qua da dưới hướng dẫn siêu âm và/hoặc CLVT, sinh thiết trong mổ. Tuy nhiên, đối với các tổn thương ở sâu, cạnh mạch máu lớn trong ổ bụng, tổn thương ở vùng rốn gan, tổn thương trong lòng đường mật, các phương pháp sinh thiết kể trên có thể không thực hiện được hoặc tiềm ẩn nhiều nguy cơ biến chứng nguy hiểm như chảy máu hay tổn thương tạng lân cận. Sinh thiết lõi khối u trong lòng đường mật qua da bằng forceps (PTFB: percutaneous transluminal forceps biopsy) là một được tích hợp thành một bước trong quy trình can thiệp dẫn lưu đường mật qua da xuyên gan (PTBD: percutaneous transhepatic biliary drainage) trong xử trí vàng da tắc mật. Trong kỹ thuật PTBD, một đường hầm qua da, xuyên gan được tạo ra để nối thông vào đường mật trong gan, từ đó luồn ống dẫn lưu vào đường mật. Kỹ thuật PTFB tận dụng đường hầm này để đưa forceps vào tiếp cận ngay tại vị trí khối u để lấy mẫu bệnh phẩm.
PTFB là một kỹ thuật an toàn và hiệu quả, được chỉ định thay thế cho những trường hợp khó tiếp cận tổn thương bằng nội soi hoặc qua da xuyên thành bụng. Kỹ thuật này có thể kết hợp với can thiệp dẫn lưu qua da giảm áp đường mật trong một thì, vừa đảm bảo yêu cầu giải quyết triệu chứng, vừa lấy mẫu bệnh phẩm để chẩn đoán nguyên nhân (7). Theo một nghiên cứu gộp, kỹ thuật PTFB có độ nhạy 81%, độ đặc hiệu 100%, giá trị chẩn đoán 85,3% đối với tắc mật ác tính (1). Tuy nhiên, đây là một thủ thuật không đơn giản, đòi hỏi có sự phối hợp của nhiều chuyên gia và chuyên khoa như Nội soi, Ngoại Tiêu hoá hoá, Chẩn đoán hình ảnh – Điện quang can thiệp, giải phẫu bệnh, ung bướu. Bệnh viện trường Đại học Y-Dược Huế là cơ sở y tế chuyên sâu được trang bị đầy đủ trang thiết bị hiện đại như máy cắt lớp vi tính 128 dãy, máy cộng hưởng từ 1.5T, hệ thống chụp mạch xoá nền DSA, forcep chuyên dụng cùng với đội ngũ nhân lực đa chuyên khoa hoàn chỉnh đã và đang từng bước hoàn thiện quy trình chẩn đoán và điều trị những bệnh lý phức tạp.
KẾT LUẬN
Sinh thiết lõi khối u trong lòng đường mật qua da bằng forceps (PTFB: percutaneous transluminal forceps biopsy) là một kỹ thuật khả thi, an toàn, có hiệu quả chẩn đoán xác định bản chất khối u. Việc triển khai thành công kỹ thuật này sẽ mở ra cơ hội điều trị trúng đích cho nhiều bệnh nhân tắc mật ác tính.
TÀI LIỆU THAM KHẢO
1. Jeon TY, Choi MH, Yoon SB, Soh JS, Moon SH. Systematic review and meta-analysis of percutaneous transluminal forceps biopsy for diagnosing malignant biliary strictures. Eur Radiol. 2022;32(3):1747-56.
2. Hristov B, Doykov D, Andonov V, Doykov M, Kraev K, Uchikov P, et al. Interventional Treatment of Malignant Biliary Obstruction: Is It Time to Change the Paradigm? Gastroenterology Insights. 2024;15(2):266-84.
3. Pavlidis ET, Pavlidis TE. Pathophysiological consequences of obstructive jaundice and perioperative management. Hepatobiliary & pancreatic diseases international : HBPD INT. 2018;17(1):17-21.
4. Cai Q, Wu X. Ultrasound-guided percutaneous transhepatic biliary drainage for distal biliary malignant obstructive jaundice. Sci Rep. 2024;14(1):12481.
5. Pu LZ, Singh R, Loong CK, de Moura EG. Malignant Biliary Obstruction: Evidence for Best Practice. Gastroenterology research and practice. 2016;2016:3296801.
6. Park JG, Jung GS, Yun JH, Yun BC, Lee SU, Han BH, et al. Percutaneous transluminal forceps biopsy in patients suspected of having malignant biliary obstruction: factors influencing the outcomes of 271 patients. Eur Radiol. 2017;27(10):4291-7.
7. Fohlen A, Bazille C, Menahem B, Jegonday MA, Dupont B, Le Pennec V, et al. Transhepatic forceps biopsy combined with biliary drainage in obstructive jaundice: safety and accuracy. Eur Radiol. 2019;29(5):2426-35.