Nguyễn Đoàn Khánh Trang1, Trần Đình Bình2*
1Học viên lớp Cao học Dược lý- Dược Lâm sàng khóa 2024-2026
2Khoa KSNK, Bệnh viện Đại học Y Dược Huế, tác giả liên hệ
I. MỞ ĐẦU
Da là một rào cản tự nhiên chống lại sự xâm nhập của vi khuẩn (VK). Tuy đã có rất nhiều biện pháp phòng ngừa và phương thức để dự phòng nhiễm trùng (NT) tại chỗ nhưng bất kỳ phẫu thuật (PT) nào đòi hỏi phải rạch da đều có nguy cơ NT nơi xảy ra PT, hay còn gọi là nhiễm khuẩn vết mổ (NKVM) và tỷ lệ này nằm trong khoảng từ 1% đến 3%, đôi khi có thể lên đến 20% [50]. Tại Việt Nam, NKVM xảy ra cao hơn so với tỷ lệ chung của khu vực: khoảng 10,9% cho Việt Nam và 7,8% cho khu vực Đông Nam Á [1].
Kháng sinh dự phòng (KSDP) được định nghĩa là một đợt kháng sinh ngắn thực hiện trên bệnh nhân (BN) ngay trước khi PT và chấm dứt trong vòng 24 giờ sau khi đóng vết mổ. Việc sử dụng KSDP có thể được coi là dự phòng tiên phát (phòng ngừa NT ban đầu) hoặc dự phòng thứ phát (phòng ngừa tái phát hoặc NT lại) NKVM bằng cách diệt trừ VK tại vị trí PT [45]. Ở các nước phát triển, KSDP đã được sử dụng phổ biến trong các PT sạch và sạch nhiễm bởi nó đem lại nhiều lợi ích trên các phương diện như làm giảm nguy cơ NKVM cho BN sau PT dẫn đến hạn chế bớt thời gian nằm viện nên sẽ tiết kiệm chi phí cho KS dài ngày hậu phẫu và viện phí, cũng như giúp giảm thiểu tình trạng kháng kháng sinh (KS) đang rất được quan tâm hiện nay. Tuy nhiên, ở Việt Nam, KSDP mới được áp dụng cách đây một vài năm và với điều kiện vệ sinh bệnh viện, vệ sinh phòng mổ chưa thật sự tốt nên các bác sĩ vẫn giữ thói quen dùng KS điều trị dài ngày cho mọi loại PT trong bệnh viện [7].
Cho đến nay, mặc dù vẫn còn nhiều ý kiến trái chiều cho rằng việc sử dụng KSDP làm gia tăng nguy cơ và làm xuất hiện các chủng vi khuẩn đề kháng kháng sinh, song theo các hướng dẫn phòng ngừa NKVM của nhiều quốc gia trên thế giới, KSDP được khẳng định là một biện pháp quan trọng và có ý nghĩa lâm sàng cụ thể trong việc phòng ngừa và làm giảm mức độ NKVM [30]. Và để KSDP phát huy được tối đa tác dụng và đem lại hiệu quả như mong muốn yêu cầu sự tuân thủ chặt chẽ theo Hướng dẫn chung của Bộ Y tế về phòng ngừa NKVM cũng như các Hướng dẫn cụ thể của mỗi bệnh viện cho việc sử dụng KSDP trong chỉ định, lựa chọn, liều dùng, đường dùng KSDP… thì vẫn có rất ít bệnh viện có thể thực hiện được.
Bài viết này được tổng hợp từ nhiều nguồn tài liệu tham khảo nhằm phân tích và trình bày về kháng sinh dự phòng, nguyên tắc sử dụng kháng sinh dự phòng và mục đích sử dụng kháng sinh dự phòng trong ngoại khoa và giới thiệu một số hướng dẫn sử dụng kháng sinh dự phòng hiện hành để các đồng nghiệp có thể tham khảo.
II. KHÁI NIỆM KHÁNG SINH DỰ PHÒNG
KSDP là kháng sinh được sử dụng trong thời gian ngắn nhằm mục đích giảm tần suất nhiễm khuẩn tại vị trí hoặc cơ quan được PT, không dự phòng nhiễm khuẩn toàn thân hoặc vị trí cách xa nơi được PT [6] [22]. KSDP được sử dụng trước khi phơi nhiễm với các tác nhân gây nhiễm khuẩn trong PT nhằm ngăn ngừa các biến chứng nhiễm khuẩn do đó phải được sử dụng ngay trước hoặc trong PT và việc kéo dài KSDP sau PT thường vô nghĩa [5] [31]. KSDP được lựa chọn có phổ bao phủ vi khuẩn gây NKVM tại vị trí PT [6] [10]. Quan điểm KSDP hiện đại cần được phân biệt với kháng sinh điều trị sớm (khi quá trình nhiễm khuẩn đã được khởi phát hoặc khi đã có ổ nhiễm khuẩn xuất hiện trong quá trình PT), và với KSDP cổ điển (mang ý nghĩa phòng vệ nhiễm trùng bao phủ các căn nguyên không xác định, các chỉ định quá rộng, việc phòng ngừa quá chậm, trễ thời gian dùng kéo dài dẫn đến kết quả phòng ngừa kém hay âm tính) [19] [25].
KSDP cần :
- Ngăn ngừa được NKVM
- Ngăn ngừa được bệnh tật và tử vong liên quan đến NKVM,
- Giảm thời gian và chi phí chăm chăm sóc
- Không gây phản ứng có hại và không gây hậu quả xấu đối với hệ sinh vật của BN và bệnh viện [15].
III. MỤC ĐÍCH SỬ DỤNG KHÁNG SINH DỰ PHÒNG TRONG NGOẠI KHOA
KSDP được sử dụng để tạo được nồng độ kháng sinh cần thiết tại vùng PT. Nồng độ kháng sinh cao là yếu tố cần để chống lại các vi khuẩn có khả năng xuất hiện tại nơi PT tương ứng [19]. KSDP sẽ hỗ trợ hệ miễn dịch làm giảm đến mức tối thiểu lượng vi khuẩn có thể gây nhiễm trùng tại vị trí PT [25]. Tóm lại, KSDP được dùng với các mục đích:
Giảm thiểu tỷ lệ NKVM
Giảm thời gian nằm viện
Giảm chi phí cho BN và bệnh viện
Giảm tình trạng kháng kháng sinh
Thuận lợi cho bác sỹ trong kê đơn thuốc
Giảm thiểu công việc điều trị cho đội ngũ điều dưỡng..
IV. HƯỚNG DẪN SỬ DỤNG KHÁNG SINH DỰ PHÒNG TRONG NGOẠI KHOA
4.1. Một số hướng dẫn sử dụng kháng sinh dự phòng
Bảng 1. Các Hướng dẫn sử dụng kháng sinh dự phòng
|
Năm ban hành |
Đơn vị ban hành |
Tên hướng dẫn |
|
2022 |
Paediatric Infectioua Disease Group of Switzerland (PIGS) |
Swiss recommendations on perioperative antimicrobial prophylaxis in children [27] |
|
2022 |
Pediatric Antimicrobial Stewardship |
Pediatric and Neonatal Surgical Prophylaxis Guidelines [12] |
|
2020 |
Bệnh viện Nhi đồng 1 |
Phác đồ Ngoại Nhi bệnh viện Nhi đồng 1, cập nhật [2] |
|
2017 |
Goverment of South Australia |
Surgical Antimicrobial Prophylaxis Clinical Guideline [22] |
|
2017 |
Global Alliance for Infections in Surgery and the World Society of Emergency Surgery |
A Global Declaration in Apporpriate Use of Antimicrobial Agents across the Surgical Pathway [20] |
|
2016 |
Bệnh viện Phụ sản - Nhi Đà Nẵng |
Hướng dẫn sử dụng kháng sinh dự phòng trong phẫu thuật ở trẻ em [3] |
|
2015 |
Bộ Y Tế Việt Nam |
Hướng dẫn sử dụng kháng sinh [6] |
|
2014 |
The Canadian Patient Satety Institue |
Prevent Surgical Site Infections Getting Started Kit [26] |
|
2014 |
SHEA, IDSA |
Strategies to Surgical Site Infections in Acute Care Hospitals: 2014 Update [11] |
|
2013 |
ASHP |
Clinical practice guidelines for antimicrobial prophylaxis in surgery [15] |
4.2. Nguyên tác sử dụng kháng sinh dự phòng
Nguyên tắc 1: Dùng KSDP khi nguy cơ nhiễm khuẩn cao
KSDP được chỉ định cho các PT sạch có kèm yếu tố nguy cơ NKVM và toàn bộ PT sạch nhiễm.
So sánh chỉ định KSDP giữa Hướng dẫn của Bộ Y tế và Hướng dẫn của bệnh viện Phụ sản - Nhi Đà Nẵng cho trẻ em ta thấy có sự tương đồng và khác biệt như trong bảng:
Bảng 2. Chỉ định kháng sinh dự phòng trong các Hướng dẫn
|
Loại PT |
Hướng dẫn của Bộ Y tế |
Hướng dẫn của bệnh viện Phụ sản - Nhi Đà Nẵng cho bệnh nhi |
|
Sạch |
√ (can thiệp ngoại khoa nặng, có thể ảnh hưởng tới sự sống còn và/hoặc chức năng sống như PT chỉnh hình, PT tim và mạch máu, PT thần kinh, PT nhãn khoa) |
√ (một số phẫu thuật nguy cơ cao như phẫu thuật tim, chỉnh hình xương...) |
|
Sạch - nhiễm |
√ |
√ |
|
Nhiễm |
|
|
|
Bẩn |
|
|
|
Lưu ý |
Không khuyến cáo cho các PT chấn thương chỉnh hình sạch ở tay, đầu gối, chân, các loại PT nội soi khớp |
|
Nguyên tắc 2: Cần lựa chọn KSDP phù hợp dựa trên các tiêu chuẩn sau:
- Có hiệu lực trên vi khuẩn nhiều khả năng làm tăng nguy cơ NKVM
- Cho nồng độ đủ tác dụng tại nơi PT
- Cho tác dụng phụ ít nhất
- Tương đối ít đắt tiền
- Không làm xáo trộn hệ vi khuẩn ở BN hay bệnh viện.
Do đó, việc lựa chọn KSDP phụ thuộc vào căn nguyên gây NKVM tại vị trí PT, dịch tễ học, tình trạng kháng thuốc ở địa phương và bệnh viện, hiệu quả, chi phí, tính an toàn của thuốc và tiền sử dị ứng của BN. Hay nói cách khác là phụ thuộc vào các yếu tố cụ thể sau:
• Yếu tố về kháng sinh:
- Nên chọn kháng sinh có phổ tác dụng phù hợp với vi khuẩn chính gây NKVM tại vị trí PT, ít có khả năng chọn lọc vi khuẩn đề kháng kháng sinh và làm thay đổi hệ vi khuẩn thường trú. Các cephalospotin thế hệ 1 và thế hệ 2 là các kháng sinh được khuyến cáo nhiều nhất trong các hướng dẫn dự phòng NKVM. Trong đó cefazolin là thuốc được chứng minh đầy đủ về hiệu quả dự phòng, đáp ứng được các tiêu chí đề ra. Đối với cephalosporin thế hệ 3, tuy phổ kháng khuẩn rộng nhưng chi phí cao nên không được khuyến khích sử dụng trong các hướng dẫn [9] [15] [16] [18].
• Yếu tố về vi sinh:
- Phổ kháng khuẩn của kháng sinh có thể bao trùm được các chủng vi khuẩn
có khả năng gây NKVM trên loại PT đang được thực hiện. Đồng thời phù hợp với tình hình đề kháng kháng sinh và dịch tễ tại địa phương cũng như tại cơ sở y tế [15] [25]. Những trường hợp NKVM do MRSA hoặc Staphylococci sinh men coagulase kháng methicilin khuyến cáo nên sử dụng vancomycin. Nhưng nếu để ngăn ngừa NKVM gây ra bởi MSSA thì cần phối hợp thêm cefazolin để tăng khả năng dự phòng [15]. Việc sử dụng hợp lý vancomycin phải được xem xét để giảm thiểu nguy cơ có thể gia tăng của vi khuẩn đường ruột kháng vancomycin (VRE) [35].
• Yếu tố về BN:
- Thận trọng với BN có tiền sử dị ứng thuốc, đặc biệt là dị ứng với kháng
sinh nhóm betalactam, kháng sinh penicilin. Cũng cần cân nhắc đến các BN suy giảm chức năng gan thận để có thể điều chỉnh liều phù hợp nhất là khi BN được chỉ định nhiều hơn một liều KSDP trong một ca mổ [6] [7] [16]. Cần tránh dùng cephalosporin cho BN tiền sử dị ứng qua trung gian IgE với penicilin và lựa chọn vancomycin hoặc clindamycin để thay thế trong trường hợp này [15].
Nguyên tắc 3:
- Đường dùng thuốc ưu tiên là đường tĩnh mạch đề thuốc được đưa trực tiếp vào hệ mạch, đạt nồng độ cần thiết trong huyết tương và mô một cách nhanh chóng và có thể tiên lượng được [15] [18]. Không ưu tiên đường tiêm bắp nhưng có thể thay thế đường tiêm tĩnh mạch nếu đảm bảo được tốc độ hấp thu của thuốc trên một số đối tượng cụ thể. Đường uống chỉ dùng cho BN PT trực tràng, đại tràng. Đường đặt trực tràng chỉ hiệu quả trong một vài PT nhất định [15].
- Liều sử dụng dựa trên trọng lượng BN. Liều KSDP tương đương liều mạnh nhất của kháng sinh đó. Liều thường sẽ cao hơn ở BN béo phì để đảm bảo nồng độ thuốc vẫn đạt được nồng độ thích hợp tại thời điểm rạch da cho đến khi PT kết thúc.
- Liều dự phòng PT cho trẻ em không được vượt quá liều thông thường cho người lớn [6].
Bảng 3. Liều dùng và đường dùng khuyến cáo của một số kháng sinh dự phòng
|
Kháng sinh |
Liều thường dùng |
Đường dùng |
|
Ampicilin/sulbactam |
3g |
Tiêm tĩnh mạch chậm |
|
Cefazolin |
< 120 kg: 2g ≥ 120 kg: 3g 30 mg/kg** |
Tiêm tĩnh mạch chậm |
|
Cefoxitin |
2g |
Tiêm tĩnh mạch chậm |
|
Cefotaxim |
50 mg/kg** |
Tiêm tĩnh mạch chậm |
|
Cefuroxim |
1,5g |
Tiêm tĩnh mạch chậm |
|
Ceftriaxon |
2g |
Tiêm tĩnh mạch chậm |
|
Ciprofloxacin |
400mg |
Truyền tĩnh mạch 1 giờ |
|
Clindamycin |
900mg* |
Tiêm tĩnh mạch chậm |
|
Metronidazol |
500mg |
Truyền tĩnh mạch 30 phút |
* Theo Hướng dẫn của Bộ Y tế là 600mg
** Theo Hướng dẫn sử dụng KSDP của bệnh viện Phụ sản - Nhi Đà Nẵng
Nguyên tắc 4: Không bắt đầu đưa thuốc quá sớm, cũng không quá muộn. Thời điểm sử dụng nên trước khi tiến hành PT và gần thời điểm rạch da để nồng độ kháng sinh đạt mức cao nhất ở thời điểm rạch da.
Bảng 4. Thời điểm khuyến cáo sử dụng kháng sinh dự phòng phẫu thuật
|
Tổ chức - thời gian ban hành |
Khuyến cáo về thời điểm sử dụng KSDP đường tiêm/truyền tĩnh mạch |
|
Bộ Y tế Việt Nam - 2015 [6] |
Trong vòng 1 giờ trước khi rạch da. Vancomycin và fluoroquinolon cần được sử dụng trong vòng 120 phút trước thời điểm rạch da do thời gian truyền thuốc kéo dài. |
|
Bệnh viện Phụ sản - Nhi Đà Nẵng [3] |
Trong vòng 30 phút trước khi rạch da. |
|
WHO - 2018 [31] |
Trước khi rạch da trong vòng 120 phút. Đối với kháng sinh có thời gian bán thải thấp là 60 trước thời điểm rạch da. |
|
ASHP - 2013 [15] |
Trong vòng 1 giờ trước khi rạch da. Riêng vancomycin và clindamycin là 120 phút trước khi rạch da. |
|
SHEA/IDSA - 2014 [11] |
Sử dụng từ 0 - 30 phút sẽ hiệu quả hơn từ 30 - 60 phút trước khi rạch da, miễn là trong vòng 1 giờ trước khi rạch da. Riêng vancomycin và clindamycin là 120 phút trước khi rạch da. |
|
The Royal College of Physicians của Ireland – 2012 [32] |
Trong vòng 1 giờ trước khi rạch da. Nếu có garo cầm máu thì sử dụng trước 15 phút so với thời điểm quấn garo. |
|
NICE - 2008 [33] |
Trước khi gây mê |
|
Bệnh viện Vinmec Times City, Việt Nam [4] |
Trong vòng 1 giờ trước khi rạch da. Tối ưu nhất là 15 - 30 phút. |
Mối liên hệ giữa thời điểm sử dụng KSDP và tỷ lệ NKVM trong một nghiên cứu trên 2.747 BN cho kết quả như trong đồ thị sau [17]:
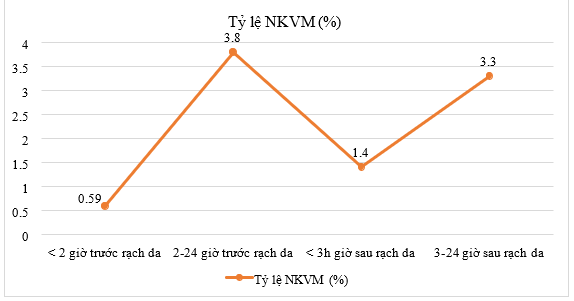
Hình 1. Thời điểm sử dụng kháng sinh dự phòng và tỷ lệ nhiễm khuẩn vết mổ
Việc sử dụng KSDP trong vòng 30 phút, từ 30 - 60 phút hay 60 - 120 phút không cho thấy sự khác biệt về mặt lợi ích và nguy cơ NKVM [31].
Nguyên tắc 5: Chỉ bổ sung liều kháng sinh trong khi PT nếu cần thiết như khi thời gian mổ kéo dài > 3 giờ hay trên 2 lần thời gian bán thải của kháng sinh hoặc BN bị mất máu nhiều trong quá trình PT (> 1.500ml ở người lớn và 25 ml/kg ở trẻ em), có thể xem xét đối với BN có BMI ≥ 30 vì thể tích phân bố rộng hơn. Khoảng cách đưa liều tiếp theo tính từ thời điểm sử dụng liều đầu tiên khi tiền mê [5] [15]. Ý nghĩa của việc lặp lại liều KSDP là để duy trì nồng độ kháng sinh > MIC trong suốt quá trình PT. Không phải tất cả các trường hợp đều cần lặp lại liều kháng sinh, ví dụ như BN suy thận vì thời gian bán thải của kháng sinh được kéo dài thêm [15]. Nếu một BN đã dùng vancomycin và bị suy thận, cefazolin nên được cân nhắc trước khi PT thay vì dùng thêm một liều vancomycin [29].
Nguyên tắc 6: Việc tiếp tục sử dụng kháng sinh sau PT nên ở mức tối thiểu. Chỉ sử dụng đến khi hết nguy cơ xâm nhập của vị khuẩn (≤ 48 giờ với PT tim mạch và ≤ 24 giờ với hầu hết các PT khác) [15, 20]; WHO-2018, CDC-2017 và Hiệp hội PT viên Hoa Kỳ 2016 đều đồng thuận khuyến cáo dừng KSDP sau khi đóng vết mổ vì lợi ích đem lại về hiệu quả của 1 liều KSDP duy nhất trước PT tương đương như KSDP kéo dài [13] [26] [31].
Sử dụng KSDP kéo dài không những không có ý nghĩa về mặt dự phòng NKVM mà còn gia tăng khả năng gặp phải ADR của thuốc, đặc biệt nghiêm trọng là nhiễm Clostridium difficile và tăng đề kháng kháng sinh đối với các kháng sinh phổ rộng [14] [21] [23]. Ngoài ra, chưa có bằng chứng lâm sàng chứng minh lợi ích của KSDP kéo dài cho đến khi rút dẫn lưu hay catheter tĩnh mạch [24].
Quyết định có sử dụng kéo dài kháng sinh sau PT còn phụ thuộc vào tình trạng vết mổ, thể trạng BN, điều kiện phòng mổ, khả năng chăm sóc hậu phẫu, tình hình dịch tễ địa phương, và ý kiến của bác sĩ.
V. KẾT LUẬN
TÀI LIỆU THAM KHẢO
TIẾNG VIỆT
APSIC. (2018). Hướng dẫn của APSIC về phòng ngừa nhiễm khuẩn vết mổ.
Bệnh viện Nhi đồng 1 (2020). Phác đồ Ngoại Nhi bệnh viện Nhi đồng 1, cập nhật (9 ed.): NXB Y học.
Bệnh viện Phụ sản Nhi - Đà Nẵng (2016), Hướng dẫn sử dụng kháng sinh dự phòng cho trẻ em.
Bệnh viện Vinmec Times City (2016), Hướng dẫn sử dụng kháng sinh dự phòng.
Bộ Y tế (2012). Hướng dẫn phòng ngừa nhiễm khuẩn vết mổ.
Bộ Y tế (2015). Hướng dẫn sử dụng kháng sinh
Nguyễn Quốc Anh (2008). Nghiên cứu một số yếu tố nguy cơ nhiễm khuẩn vết mổ tại bệnh viện Bạch Mai. (Doctor). Trường Đại học Y Hà Nội, Hà Nội.
Vũ Hồng Khánh (2022). Triển khai chương trình kháng sinh dự phòng trong phẫu thuật chấn thương chỉnh hình sạch tại khoa chấn thương chỉnh hình và y học thể thao, bệnh viện Đại học Y Hà Nội. (Master). Trường Đại học Dược Hà Nội.
TIẾNG ANH
Aj, M. (1999). Guideline for prevention of surgical site infection, 1999. Centers for disease control and prevention (CDC) hospital infection control practices advisory committee. Am J Infect Control, 27(2), 97- 132, quiz 133-134, discussion 196.
American Society of Health-System Pharmacists (1999). ASHP therapeutic guidelines on antimicrobial prophylaxis in surgery. Am J Health Syst Pharm, 56, 1839-1888.
Anderson, D. J., Podgorny, K., Berríos-Torres, S. I., Bratzler, D. W., Dellinger, E. P., Greene, L., . . . Maragakis, L. L. (2014). Strategies to prevent surgical site infections in acute care hospitals: 2014 update. Infection Control & Hospital Epidemiology, 35(S2), S66-S88.
Avocate Children Hospital (2022). Pediatric and Neonatal Surgical Prophylaxis Guidelines. Retrieved 17/03/2023
Berríos-Torres, S. I., Umscheid, C. A., Bratzler, D. W., Leas, B., Stone, E. C., Kelz, R. R, Mazuski, J. E. (2017). Centers for disease control and prevention guideline for the prevention of surgical site infection, 2017. JAMA surgery, 152(8), 784-791.
Bratzler, D. W., Dellinger, E. P., Olsen, K. M., Perl, T. M., Auwaerter, P. G., Bolon, M. K., . . . Slain, D. (2013). Clinical practice guidelines for antimicrobial prophylaxis in surgery. Surgical infections, 14(1), 73-156.
Bratzler, D. W., Houck, P. M., Richards, C., Steele, L., Dellinger, E. P., Fry, D. E., . . . Red, L. (2005). Use of antimicrobial prophylaxis for major surgery: baseline results from the National Surgical Infection Prevention Project. Archives of Surgery, 140(2), 174-182.
Cate Whittlesea, K. H. (2019). Clinical Pharmacy and Therapeutics s(pp. 596 - 605).
Classen, D. C., Evans, R. S., Pestotnik, S. L., Horn, S. D., Menlove, R. L., & Burke, J. P. (1992). The timing of prophylactic administration of antibiotics and the risk of surgicalwound infection. New England Journal of Medicine, 326(5), 281-286.
Dipiro, J. T., Talbert, R. L., Yee, G. C., Matzke, G. R., Wells, B. G., & Posey, L. M. (20120). Pharmacotherapy: a pathophysiologic approach (11 ed.): McGraw-Hill Education.
European Centre for Disease Prevention and Control (ECDC). (2013). Systematic review and evidence-based guidance on perioperative antibiotic prophylaxis: ECDC.
Global Alliance for Infections in Surgery Working Group (2017). A global declaration on appropriate use of antimicrobial agents across the surgical pathway. Surgical infections, 18(8), 846-853.
Harbarth, S., Samore, M. H., Lichtenberg, D., & Carmeli, Y. (2000). Prolonged antibiotic prophylaxis after cardiovascular surgery and its effect on surgical site infections and antimicrobial resistance. Circulation, 101(25), 2916-2921.
Ierano, C., Nankervis, J.-A. M., James, R., Rajkhowa, A., Peel, T., & Thursky, K. (2017). Surgical antimicrobial prophylaxis. Australian prescriber, 40(6), 225.
Kirkwood, K. A., Gulack, B. C., Iribarne, A., Bowdish, M. E., Greco, G., Mayer, M. L., . . . Ghanta, R. K. (2018). A multi-institutional cohort study confirming the risks of Clostridium difficile infection associated with prolonged antibiotic prophylaxis. The Journal of thoracic and cardiovascular surgery, 155(2), 670-678. e671.
McCarthy, P. J., Patil, S., Conrad, S. A., & Scott, L. K. (2010). International and specialty trends in the use of prophylactic antibiotics to prevent infectious complications after insertion of external ventricular drainage devices. Neurocritical care, 12, 220-224.
Nichols, R. L. (2001). Preventing surgical site infections: a surgeon's perspective. Emerging infectious diseases, 7(2), 220.
Now, S. H. (2014). Prevent Surgical Site Infections Getting Started Kit. Edmonton: Canadian Patient Safety Institute.
Paioni, P., Aebi, C., Bielicki, J., Buettcher, M., Crisinel, P. A., Kahlert, C. R., . . . Berger, C. (2022). Swiss recommendations on perioperative antimicrobial prophylaxis in children. Swiss medical weekly, 152(3738), w30230-w30230.
Sartelli, M., Duane, T. M., Catena, F., Tessier, J. M., Coccolini, F., Kao, L. S., . . . Ansaloni, L. (2016). Antimicrobial stewardship: a call to action for surgeons. Surgical infections, 17(6), 625-631.
Ter Gunne, A. F. P., Hosman, A. J., Cohen, D. B., Schuetz, M., Habil, D., Van Laarhoven, C. J., & Van Middendorp, J. J. (2012). A methodological systematic review on surgical site infections following spinal surgery: part 1: risk factors. Spine, 37(24), 2017-2033.
Unger, N. R., & Stein, B. J. (2014). Effectiveness of pre-operative cefazolin in obese patients. Surgical Infections, 15(4), 412-416.
Wagenlehner, F., Stöwer-Hoffmann, J., Schneider-Brachert, W., Naber, K. G., & Lehn, N. (2000). Influence of a prophylactic single dose of ciprofloxacin on the level of resistance of Escherichia coli to fluoroquinolones in urology. Int J Antimicrob Agents, 15(3), 207211. doi:10.1016/s0924-8579(00)00182-5
WHO (2018). Global guidelines for the prevention of surgical site infection, 2nd edition: World Health Organization.
Woodcock, T., Barker, P., Daniel, S., Fletcher, S., Wass, J., Tomlinson, J., . . . Vercueil, A. (2020). Guidelines for the management of glucocorticoids during the peri‐operative period for patients with adrenal insufficiency: Guidelines from the Association of Anaesthetists, the Royal College of Physicians and the Society for Endocrinology UK. Anaesthesia, 75(5), 654-663.
Wray, D., Ruiz, F., Richey, R., & Stokes, T. (2008). Prophylaxis against infective endocarditis for dental procedures–summary of the NICE guideline. British dental journal, 204(10), 555-557.
WEBSITE
Crader MF, V. M. (Updated 2022 Sep 4). Updated 2022 Sep 4. In. Retrieved from https://www.ncbi.nlm.nih.gov/books/NBK442032/, accessed 01/10/2025.